
par Audrey Vaugrente

par Audrey Vaugrente
Deux fabricants de dispositifs et implants médicaux ont distribué des produits ne se conformant pas aux règles européennes. Alors que le certificat de conformité CE est obligatoire, ils ont triché pendant près de deux ans. En toute impunité.
Les dispositifs et implants médicaux doivent faire l’objet d’un contrôle plus strict. Une récente vague de rappels le confirme, peu après l’affaire des « implant files ». Deux fabricants ont retiré du marché plusieurs centaines de leurs produits. Une nouvelle illustration des manquements réguliers dans ce domaine. Ils ne disposaient pas d’un marquage CE conforme… et ce depuis 2016 ! Il s’agit pourtant d’une condition indispensable à leur distribution dans l’Union européenne (1).
C’est d’abord la société américaine Zavation qui a contacté l’Agence nationale de sécurité du médicament (ANSM). À l’occasion d’un rachat, elle s’est rendu compte que sa nouvelle conquête, Pan Medical US Corporation, n’avait pas respecté les règles de mise sur le marché européen. « L’ancien propriétaire a falsifié les dates d’expiration des certifications de marquage CE », explique Zavation dans un courrier adressé aux professionnels de santé. L’ensemble des produits fabriqués entre août 2016 et octobre 2018 sont concernés par cette manœuvre, et sont donc retirés du marché. Il s’agit de dispositifs d’aide à l’intervention ou encore de ciments destinés à combler les vertèbres fracturées. La plupart ne sont pas destinés à rester dans l’organisme des personnes opérées.
Le lendemain, l’entreprise CL Medical a fait l’objet d’un rappel à l’ordre de la part de l’ANSM pour des raisons similaires. Aucune trace d’un certificat de conformité CE pour 130 lots d’implants de renfort (2) indiqués dans le traitement de l’incontinence urinaire ou du prolapsus génito-urinaire (ou descente d’organes) pendant un peu moins de deux ans. La mise sur le marché des modèles fabriqués jusqu’au 31 janvier 2018 est suspendue.
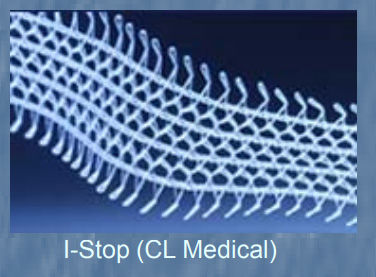
Dans sa décision de police sanitaire, l’Agence souligne que le précieux certificat a expiré le 23 novembre 2016. Bien qu’obligatoire, il n’a pas été renouvelé avant le 1er février 2018… Dans l’intervalle, les implants ont tout de même été vendus et posés chez des hommes et des femmes. C’est ce qui explique cette mesure officielle. Car « en l’absence de certificat CE délivré par un organisme notifié, la conformité des dispositifs aux exigences essentielles n’est pas démontrée, indique le jugement de l’ANSM. En conséquence, leur sécurité d’utilisation n’est pas garantie. » Cependant, l’Agence précise qu’aucun risque pour la santé des personnes portant un tel implant n’a été identifié.
Même sans répercussions sanitaires, de tels manquements sont graves. Le code de la Santé publique prévoit de lourdes sanctions financières à l’encontre des entreprises qui ne respectent pas le processus de mise sur le marché des dispositifs et implants médicaux. Dans les faits, celles-ci restent rares. En 2016, seules 3 ont été prononcées sur les 17 procédures lancées par l’ANSM.
Les dispositifs médicaux les plus à risque, comme les implants, sont encore mal contrôlés. Ces derniers sont particulièrement à risque car ils restent dans l’organisme de plusieurs mois à plusieurs années. C’est pourquoi un collectif d’associations, dont l’UFC-Que Choisir, a donc réclamé une évolution de la législation. L’objectif : mettre fin au système de certification CE pour soumettre les produits les plus sensibles à une autorisation de mise sur le marché (AMM), sur le modèle des médicaments. Une telle mesure placerait, en outre, les dispositifs médicaux sous la tutelle directe des autorités publiques.
(1) Article L. 5211-3 du code de la Santé publique.
(2) Les références concernées par cette décision de police sanitaire sont disponibles sur le site de l’ANSM ; elles correspondent aux modèles I-STOP, I-STOP TOMS, PELVI-STOP et PARIE-STOP.

Audrey Vaugrente




La force d'une association tient à ses adhérents ! Aujourd'hui plus que jamais, nous comptons sur votre soutien. Nous soutenir

Recevez gratuitement notre newsletter hebdomadaire ! Actus, tests, enquêtes réalisés par des experts. En savoir plus
