
par Audrey Vaugrente

par Audrey Vaugrente

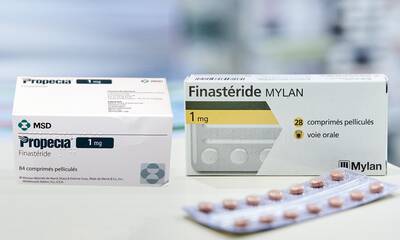
Médicament prescrit contre la chute de cheveux chez l’homme, le finastéride (Propecia) peut entraîner des effets indésirables lourds et persistants. Dans l’espoir d’en sécuriser l’usage, les autorités sanitaires renforcent les conditions dans lesquelles il pourra être délivré.
Dépression, tendances suicidaires, troubles sexuels – parfois persistants : les effets indésirables pouvant accompagner la prise de finastéride (Propecia) s’avèrent lourds. Reconnus depuis quelques années, ils ont fait l’objet de diverses mesures censées améliorer l’information des hommes souffrant d’alopécie androgénétique.
Au niveau européen, la notice accompagnant les comprimés a été revue fin 2025 pour faire apparaître le risque suicidaire. L’évolution plus récente entrera en vigueur le 16 avril : le médicament ne pourra être délivré que si le patient a signé une attestation d’information partagée. Celle-ci liste les divers effets indésirables du produit ainsi que ses bénéfices limités. « Nous rappelons régulièrement dans nos communications que le finastéride est destiné aux hommes de 18 à 41 ans atteints d’une alopécie androgénétique de stade précoce et qu’il ne fait que stabiliser la chute du cheveu. Il n’est pas indiqué chez les femmes, et ne sert à rien sur les formes avancées », insiste le Dr Philippe Vella, directeur médical à l’Agence nationale de sécurité du médicament (ANSM).
« C’est une étape nécessaire, que nous demandions depuis longtemps, se réjouit Sylviane Millon-Mathieu, fondatrice de l'association Aide aux victimes du finastéride (AVFIN), qui a participé à l’élaboration du document. Encore beaucoup de patients ne connaissent pas les effets indésirables de ce médicament. » Autre point fort de ce document : il n’élude pas les bénéfices plus que modestes du finastéride. En effet, il ne bénéficie qu’à la moitié des patients et uniquement sur le sommet du crâne. La repousse, autour de 11 %, ne se maintient pas après l’arrêt du traitement.
Cette mesure sera-t-elle efficace ? Le finastéride n’étant pas remboursé, il est impossible de savoir exactement combien d’hommes y sont exposés et si ce nombre recule. Mais les exemples précédents permettent d’en douter : la signature d’un accord de soins est aussi obligatoire pour les femmes traitées pour une acné par isotrétinoïne (Curacné, Roaccutane). Depuis 2015, la prescription initiale est également limitée aux spécialistes. Pourtant, en 2020 encore, l’Agence nationale de sécurité du médicament (ANSM) déplorait : « En dépit des mesures mises en place […], le nombre de grossesses, chez des femmes traitées exposant les enfants à naître à des risques de malformations graves, reste élevé. » Interrogée sur l’impact de ces attestations, l’agence précise que cet accord de soins ne conditionne pas l’accès au médicament, et se réfère plutôt aux résultats des mesures encadrant la prescription du valproate, antiépileptique responsable de troubles du développement s’il est pris pendant la grossesse (voir encadré).
Autre axe de travail important pour l’AVFIN, une meilleure évaluation des effets indésirables, qui s’appuie sur des données actualisées des différents patients les ayant signalés. « Beaucoup de victimes ont peur de déclarer ou n’en voient pas l’utilité, et ne mettent pas à jour leur statut. Ils sont donc considérés comme guéris, même si ce n’est pas le cas », souligne Sylviane Millon-Mathieu. Elle plaide aussi pour la reconnaissance d’une pathologie liée aux inhibiteurs de 5-alpha-réductase, dont le finastéride fait partie, qui inclut l’ensemble des effets durables. Ceux-ci ont encore peu fait l’objet de recherches scientifiques.
→ Lire aussi : Médicament - Déclarer un effet secondaire
S’il est très connu pour son effet cosmétique, le finastéride est aussi prescrit contre l’hypertrophie bénigne de la prostate, à un dosage plus élevé et sous le nom Chibro Proscar. C’est aussi le cas du dutastéride (Avodart). Ces patients aussi peuvent souffrir des effets indésirables signalés. Il est important qu’eux aussi les signalent, en passant par la plateforme dédiée.
Quel est l’impact d’une telle mesure ?
Il est difficile d’apprécier l’impact de ce type de mesure, qui fait partie de tout un ensemble de dispositions prises pour augmenter l’information des prescripteurs et des patients, et pour limiter la population exposée. Cette attestation d’information partagée a déjà été mise en place pour les femmes traitées par valproate (Dépakine, Dépakote, etc.), médicament utilisé dans l’épilepsie ou le trouble bipolaire. On a constaté une baisse de l’exposition : on est passé de 87 000 femmes traitées en 2015 à 28 000 en 2024. L’effet sur les grossesses est aussi significatif : de 1 250 grossesses exposées, on arrive à 176 en 2024. Mais l’attestation n’est pas la seule mesure mise en place.
Peut-on espérer la même chose pour le finastéride ?
C’est plus compliqué d’évaluer l’impact pour le finastéride, qui n’est pas remboursé. Faute de connaître le nombre de patients exposés, on peut suivre le nombre de boîtes vendues. Depuis 2019, il est stable. Si les ventes baissent, tant mieux, ce serait le signe que la prescription est modulée par la réflexion des patients. Mais notre premier objectif reste une meilleure information des patients et des professionnels de santé. Cela devrait diminuer l’errance des patients victimes d’effets indésirables.
Ces mesures s’appliquent-elles aussi au finastéride et au dutastéride prescrits contre l’hypertrophie bénigne de la prostate ?
La notice a aussi été modifiée pour ces médicaments, à l’issue de la réévaluation européenne de leur rapport bénéfice-risque. Mais l’Agence européenne du médicament (EMA) n’a pas jugé nécessaire d’ajouter une carte patients à la boîte. Il faut quand même souligner que le public n’est pas du tout le même que pour le finastéride : la population est plus âgée, peut déjà avoir des troubles sexuels liés à l’âge ou à l’hypertrophie de la prostate, et des troubles de l’humeur liés à l’âge ou à la pathologie. Il est donc plus difficile de faire la part des choses.

Audrey Vaugrente



La force d'une association tient à ses adhérents ! Aujourd'hui plus que jamais, nous comptons sur votre soutien. Nous soutenir

Recevez gratuitement notre newsletter hebdomadaire ! Actus, tests, enquêtes réalisés par des experts. En savoir plus
